Geschichte der Insulintherapie und die Physiologie des Insulins
Die Entdeckung von Insulin jährte sich 2021 zum hundertsten Mal. Vor genau einem Jahrhundert begann die Geschichte der Insulintherapie. Dieses wichtige Ereignis brachte eine einschneidende Veränderung für die Diabetes-Prognose. Die Entwicklung der Insulintherapie bietet heute den Menschen mit Diabetes die Möglichkeit, ein weitgehend normales Leben zu führen. Die neuesten Innovationen, mit denen die Insulin-Abgabe automatisiert und individuell geregelt werden kann, haben das Ziel, die psychische Belastung von Menschen mit Diabetes (besonders mit Typ 1) zu reduzieren und bieten ihnen die Möglichkeit, weniger Zeit auf das Management ihrer chronischen Krankheit zu verwenden und somit mehr Zeit für Dinge zu haben, die ihnen wichtig sind.
Lassen Sie uns zusammen die wichtigsten Entdeckungen und Innovationen nachvollziehen, die in der Geschichte der Insulintherapie kennzeichnend waren.
Zunächst gehen wir zurück zu den Grundlagen und sprechen über die Physiologie des Insulins, um die Insulintherapie bei Menschen mit Diabetes Typ 1 besser verstehen zu können und ebenfalls die Geschichte der Insulintherapie mit ihren innovativen Lösungen für die Diabetes-Behandlung heutzutage.
Die Physiologie des Insulins
Bei Menschen, die keinen Diabetes haben
Das Insulin wird von den Beta-Zellen der Bauchspeicheldrüse abgegeben.
Alle Zellen, die Hormone erzeugen (oder endokrine Zellen), sind in den Langerhansinseln gebündelt, die 2% der Masse des Pankreas darstellen. Die β (Beta) – Zellen der Insel produzieren also das Insulin, das ursprünglich in Form von Proinsulin erzeugt wird. Je nach Bedarf spaltet sich das Proinsulin ein zwei Teile auf:
- das C-Peptid,
- das Insulin: wenn es ins Blut abgegeben wird, wirkt es hauptsächlich in der Leber, in den Muskeln und im Fettgewebe.
Zusätzlich zu den β-Zellen enthält die Insel auch folgende Zellen:
- ⍺ (alpha) → Glucagon,
- δ (omega) → Somatostatin,
- PP → Pankreas-Polypeptid.
Bei Personen, die keinen Diabetes haben, geht die Nahrungsaufnahme bei einer Mahlzeit (und insbesondere von Kohlenhydraten) mit einem Anstieg des Glukosespiegels im Blut (Glykämie) einher, der sehr schnell die Freisetzung von Insulin durch die β-Zellen in den Langerhansinseln auslöst.
Wenn es ausgeschüttet wurde, bewirkt Insulin, dass die Glukose aus dem Blut zur Energiegewinnung in die Zellen wandert, wodurch der Blutzuckerspiegel dann wieder absinkt.
In der Leber fördert das Insulin die Speicherung von Glukose in Form von Glukogen, aber auch die Proteinproduktion in den Muskeln und die Einlagerung von Fetten im Fettgewebe.
| HÄTTEN SIE ES GEWUSST?
> Insulin ist das einzige Hormon im Organismus mit hypoglykämischer (blutzuckersenkender) Wirkung1. > Durchschnittlich ist Insulin die sechstteuerste Flüssigkeit der Welt, noch vor Quecksilber oder auch menschlichem Blut und kostet über 2 000 Euro pro Liter2. |
Andere Hormone, diesmal mit hyperglykämischer Wirkung, schalten sich ein, um den Blutzuckerspiegel aufrecht zu erhalten, darunter das Glucagon, das wiederum von den ⍺-Zellen der Inseln ausgeschüttet wird, wenn der Blutzuckerspiegel sinkt.
Durch die Modulation der Wirkung dieser Hormone je nach Blutzuckerspiegel kann dieser in einem Bereich gehalten werden, dessen Werte als normal angesehen werden.
Obgleich Insulin in großen Mengen während der Mahlzeiten ausgeschüttet wird, wird es auch gebraucht, um den Grundumsatz des Organismus sicherzustellen (Grundfunktionen außerhalb der Mahlzeiten).
Obgleich Insulin in großen Mengen während der Mahlzeiten ausgeschüttet wird, wird es auch gebraucht, um den Grundumsatz des Organismus sicherzustellen (Grundfunktionen außerhalb der Mahlzeiten).
Bei Menschen, die mit Diabetes mellitus leben
Bei Menschen mit Diabetes ist die Regulierung der Insulinausschüttung gestört. Beim Typ-1-Diabetes findet überhaupt keine Insulinausschüttung statt. Beim Typ-2-Diabetes ist die anfängliche Insulinausschüttungs-Phase beeinträchtigt, sodass das freigesetzte Insulin nicht ausreicht, um den Blutzuckerspiegel wieder auf die gewünschten Werte zurückzubringen, er bleibt also hoch, besonders nach den Mahlzeiten.
Wenn gar kein oder zu wenig Insulin vorhanden ist, kann der Organismus seinen „natürlichen Kraftstoff” (die Glukose) nicht mehr nutzen, denn dieser gelangt nicht mehr in die Zellen.
Der Organismus muss also auf Reserve-„Kraftstoffe” zurückgreifen: Fette und Eiweiße. Dazu mobilisiert das Fettgewebe seine Reserven (Triglyzeride, Fettsäuren und Glycerol) und die Muskeln bauen ihre Proteine (Aminosäuren) ab. Die Leber baut schnell ihre Glykogenreserven zu Glukose ab und bindet Aminosäuren und Glycerol, um sie in Glukose umzuwandeln. Sie bindet auch Fettsäuren und wandelt sie in Ketonkörper um, die dann ins Blut gelangen. Die Muskeln nehmen keine Glukose mehr auf und es entwickelt sich ein Anstieg des Blutzuckerspiegels (Hyperglykämie). Wenn der Insulinmangel signifikant und lang anhaltend ist, wird nicht nur ein Anstieg des Blutzuckerspiegels beobachtet, sondern auch das Vorhandensein von Ketonkörpern im Blut und auch im Urin werden Glukose und Ketonkörper nachgewiesen.
Geschichte der Insulintherapie: eine von wichtigen Entdeckungen geprägte Entwicklung
Die Anfänge des synthetischen Insulins: Insulin tierischer Herkunft
Die ersten Insuline wurden aus den Bauchspeicheldrüsen von Schweinen und Kühen isoliert und aufgereinigt. Man sprach damals von „gewöhnlichem” Insulin, das in 3 oder 4 Injektionen täglich mit Hilfe von Glasspritzen verabreicht wurde, deren Nadeln ziemlich dick waren, und das Präparat musste im Kühlschrank aufbewahrt werden.
In den 1930er bis 50er Jahren wurde es durch verschiedene Verfahren möglich, Insulinformen mit „Depot”-Wirkung zu erzeugen, die in Fläschchen und mit Spritzen verabreicht wurden. Dieses Insulin war jedoch nur unvollkommen aufgereinigt. Die Verunreinigungen waren für Allergien oder lokale Reaktionen an den Injektionsstellen verantwortlich; weiterhin wurden eine größere Häufigkeit von Lipodystrophien und die Produktion von Antikörpern gegen Insulin festgestellt, was zu einer verringerten Wirksamkeit des Insulins führte.
In den 1970er Jahren ergab die Beseitigung dieser Verunreinigungen tierische Insuline, die durch Chromatographie „gereinigt” und Monopic oder Einkomponenten genannt wurden. Man spricht dann von „hochreinem Insulin”.
Reproduktion von menschlichem Insulin durch ein chemisches Verfahren
Die chemische Struktur des menschlichen Insulins wurde 1955 von dem Biochemiker F. Sanger beschrieben.
In den 1980er Jahren wurde das tierische Insulin durch das Äquivalent des menschlichen Insulins ersetzt. Es wurde durch die Umwandlung von Schweineinsulin bei einem chemischen Verfahren (Halbsynthese) gewonnen und später durch gentechnische Verfahren (Biosynthese) aus Bakterien oder Hefen hergestellt. Welchen Nutzen hat dieses Vorgehen? Diese bedeutende Innovation ist mit dem menschlichen Insulin identisch und hat den Vorteil, dass man nicht mehr von einer tierischen Quelle abhängig war, das Risiko der Antikörperbildung reduziert ist, und vor allem, dass Insulin nun in unbegrenzten Mengen zur Verfügung stand.
Insulinanaloga
Die Veränderung der Zusammensetzung des synthetischen Insulins führte in den 1990er Jahren zu einer Veränderung seiner Wirkungsgeschwindigkeit und Wirkungsdauer. Man spricht von modifiziertem Insulin oder Insulinanaloga, die durch Biosynthese hergestellt werden. Man unterscheidet zwischen „schnellen Analoga”: schneller Wirkungseintritt und kurze Wirkungsdauer im Vergleich zu menschlichem Insulin; und „Analoga mit Depotwirkung”: intermediär oder lang wirkendes Insulin.
1993 wurden die Resultate des Diabetes Control and Complications Trial (DCCT) veröffentlicht: Demnach ermöglicht es die Reduzierung der chronischen Hyperglykämie, die nach dem HbA1c Wert beurteilt wird, den langfristigen Komplikationen des Typ-1-Diabetes (Netzhaut, Nieren, Nerven) vorzubeugen. Diese Ergebnisse sprechen also für die Notwendigkeit, den Blutzuckerspiegel gut unter Kontrolle zu halten.
Das ist der Beginn der „durch Mehrfach-Injektionen intensivierten” Insulinbehandlungen. Das Konzept der therapeutischen Aufklärung, dessen Zielsetzung darin besteht, Menschen mit Diabetes die Mittel zum Umgang mit ihrer chronischen Krankheit an die Hand zu geben, setzt sich in der Versorgung immer mehr durch (Glukosemessung etc.).
Derzeit werden alle Insuline gentechnologisch als rekombinantes Medikament hergestellt. Sie haben genau dieselbe Zusammensetzung wie das menschliche Insulin, oder bei den „Analoga” eine modifizierte Zusammensetzung, um die Wirkungsdauer zu verkürzen oder zu verlängern. Je nach Wirkungsdauer und Schnelligkeit des Wirkungseintritts unterscheidet man drei Insulin-Formen:
- langwirkend (über 24 Stunden),
- mittlere Wirkungsdauer (12 Stunden),
- schnellwirkend (2 bis 4 Stunden).
Geschichte der Insulintherapie: innovative Lösungen
Geräte zum Management des Diabetes: Insulinpumpen, Insulinpens und Blutzuckermessgeräte
In den 80er Jahren kommt die Insulinpumpe auf. Sie gibt ständig Insulin an den Organismus ab und ahmt so die Bauchspeicheldrüsenfunktion einer Person nach, die keinen Diabetes Typ 1 hat.
Gleichzeitig bieten die ersten Pens mit Insulinpatrone die Möglichkeit, auf Benutzung von Spritzen und Fläschchen weitgehend zu verzichten. Darauf folgten vorgefüllte Einweg-Insulinspritzen, ein einfacheres Mittel, sich Insulin zu injizieren, das „Insulinpen” genannt wird. Ein Wendepunkt in der Geschichte der Insulintherapie: Damit haben die Glasspritzen und die Wiederverwendung der in kochendem Wasser sterilisierten Nadeln ein Ende.
Außerdem werden die ersten Kapillar-Blutzuckermessgeräte immer kleiner und ausgereifter, und es sind nur winzige Blutstropfen erforderlich, damit sie funktionieren. Die Zuverlässigkeit nahm zu.
Kontinuierliche Glukosemessung
Die Blutzucker-Selbstmessung stellt ebenfalls einen großen Schritt nach vorn in der Geschichte der Insulintherapie dar, und zwar mit dem Aufkommen der ersten kontinuierlichen Glukosemessgeräte (CGM), die mehrmals täglich eine fast sofortige Kontrolle des interstitiellen Glukosespiegels ermöglichen, der den Werten des Kapillar-Blutzuckerspiegels sehr nahekommt.
Hilfsmittel und Techniken: Welche stehen heute zur Verfügung?
Die Menschen, die mit Diabetes (vorwiegend Diabetes Typ 1) leben, verabreichen sich das Insulin selbst subkutan. Je nach Wirkungsweise verwenden sie: ein Insulin mit langer, mittlerer oder Depotwirkung, um den Insulin-Grundbedarf abzudecken und ein kurz und schnell wirkendes Insulin für die Mahlzeiten. Die Kombination von langwirkendem und schnellem Insulin ermöglicht es, der Insulin-Physiologie im Organismus nahe zu kommen und hat das Ziel, den Zuckerspiegel im normalen Bereich zu halten.
Die schnellen „Insulinanaloga” erlauben einen kürzeren Zeitraum zwischen der Injektion und der Mahlzeit, vor allem außerhalb der eigenen Wohnung (Restaurant, Kantine, Schnellrestaurant etc.). Dadurch wurde auch die Entwicklung der „funktionellen Insulintherapie” oder das angelsächsische „carbohydrate counting” möglich, das auf einer Schätzung der Insulindosis für die Mahlzeit je nach der Menge der verzehrten Kohlenhydrate beruht. Eine kürzere Wirkungszeit verringert die Gefahr von Hypoglykämien außerhalb der Mahlzeiten oder zwischen zwei Mahlzeiten, falls mehrere Dosen verabreicht werden.
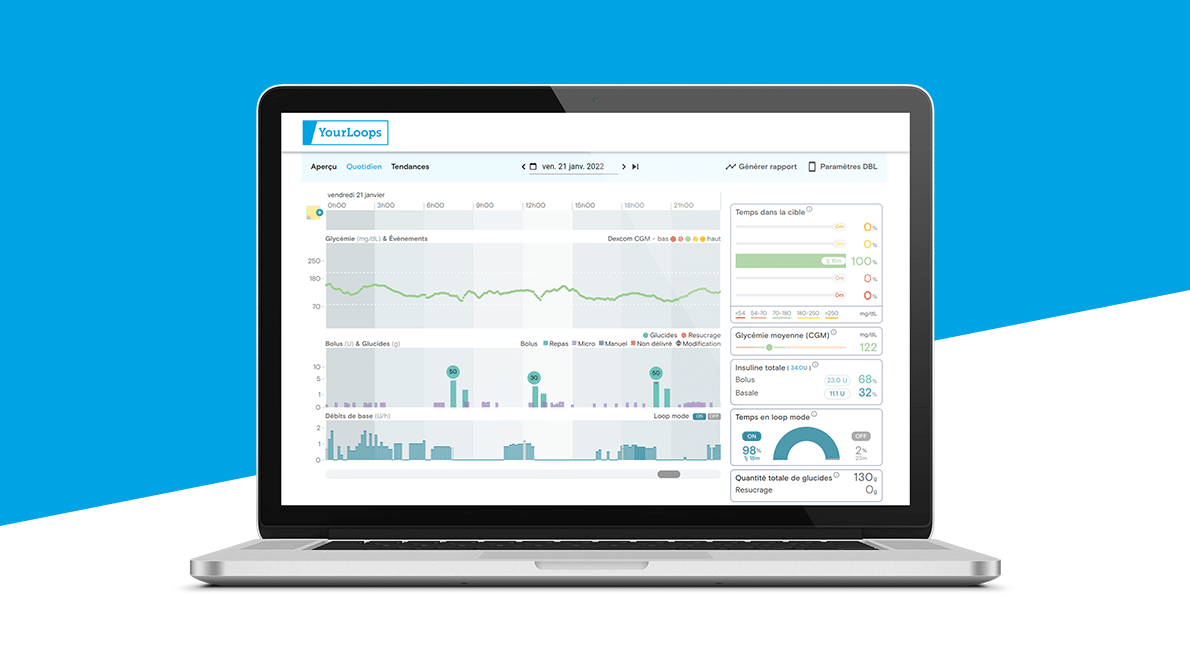
Der Einsatz von subkutanen Insulinpumpen, die nur schnelles Insulin verwenden, ziehen großen Nutzen aus den neuen Insulinen, die schneller und kürzer wirken, vor allem im Hinblick auf automatische Insulin-Abgabesysteme (auch „Closed-Loop” oder „Semi-Closed-Loop” genannt), die einen Algorithmus zur Entscheidungshilfe, ein kontinuierliches Glukosemessgerät (CGM) und eine Insulinpumpe miteinander verbinden. Die Abgabe von Insulin erfolgt dann automatisch und wird an die Werte angepasst, die von der kontinuierlichen Glukosemessungslösung übertragen werden.
In bestimmten, genau definierten Fällen wird auch in spezialisierten Zentren eine Insulinzufuhr durch eine Transplantation von Langerhansinseln erwogen.3, 4, 5, 6
BIBLIOGRAFIE
- J. Girard. Les actions physiologiques de l’insuline. MÉDECINE DES MALADIES MÉTABOLIQUES. Vol 2 – N° S2. P. 124-129 – 12/2008
- https://beyondtype1.org/the-10-most-expensive-liquids-in-the-world/#:~:text=Insulin%20%249%2C400*%20per%20gallon,produce%20in%20its%20biosynthetic%20form.
- G. Slama. Histoire de l’insulinothérapie. MÉDECINE DES MALADIES MÉTABOLIQUES. Vol 6 – N° 4. P. 352-357 – 09/2012
- Nathan DM. Long-term complications of diabetes mellitus. N Engl J Med 1993;328:1676-85.
- B.Vialettes, D.Raccah. Les analogues de l’insuline. JOHN LIBBEY EUROTEXT. 2006
- S. Halimi, N. Wion, A.-L. Coulon, P.-Y. Benhamou. Les insulines, ultra-rapides, et techniques pour accélérer l’action des insulines rapides. MÉDECINE DES MALADIES MÉTABOLIQUES. Volume 8, Issue 2, Pages 125-132. 07/2014.